An allogeniczny przeszczep komórek macierzystych to intensywna terapia polegająca na przeszczepieniu komórek macierzystych dawcy (obcej osoby). Inaczej jest w przypadku, gdy pacjent otrzymuje z powrotem własne komórki, co nazywa się an autologiczny przeszczep komórek macierzystych. Jest to omówione na innej stronie.
Przegląd allogenicznych przeszczepów komórek macierzystych?
Dr Amit Khot, hematolog i lekarz zajmujący się przeszczepami szpiku kostnego
Peter MacCallum Cancer Center i Royal Melbourne Hospital
Allogeniczny przeszczep komórek macierzystych wykorzystuje komórki macierzyste pobrane od dawcy (kogoś innego) w celu zastąpienia własnych komórek macierzystych. Ma to na celu leczenie chłoniaka, który jest oporny (nie reaguje na leczenie) lub nawracający (chłoniak, który powraca). Większość osób z chłoniakiem nie wymaga przeszczepu komórek macierzystych. W przypadku chłoniaka przeszczepy allogeniczne (dawcy) są znacznie rzadsze niż przeszczepy autologiczne ( samo) przeszczepy.
Chłoniak to nowotwór limfocytów. Limfocyty to rodzaj białych krwinek, które rozwijają się z komórek macierzystych. Cel chemoterapia jest wyeliminowanie komórek chłoniaka i wszystkich komórek macierzystych, które potencjalnie mogą przekształcić się w chłoniaka. Po wyeliminowaniu złych komórek mogą odrosnąć nowe komórki, które, miejmy nadzieję, nie są nowotworowe.
W przypadku osób z nawrotowym lub opornym na leczenie chłoniakiem to nie działa – mimo leczenia wciąż rośnie więcej chłoniaków. Dlatego wyeliminowanie komórek macierzystych za pomocą bardzo wysokich dawek chemioterapii, a następnie zastąpienie komórek macierzystych tej osoby komórkami innej osoby może skutkować nowym układem odpornościowym, w którym komórki macierzyste dawcy przejmują rolę wytwarzania komórek krwi, które nie przekształcają się w chłoniaka.
Cel przeszczepu komórek macierzystych
Istnieje wiele powodów, dla których pacjenci z chłoniakiem mogą potrzebować przeszczepu komórek macierzystych, które obejmują:
- W leczeniu pacjentów z chłoniakiem, którzy są w remisji, ale istnieje u nich „wysokie ryzyko” nawrotu chłoniaka
- Chłoniak powrócił po początkowym standardowym leczeniu pierwszego rzutu, dlatego stosuje się bardziej intensywną (silniejszą) chemioterapię, aby przywrócić remisję (brak wykrywalnej choroby)
- Chłoniak jest oporny (nie odpowiada całkowicie) na standardowe leczenie pierwszego rzutu w celu uzyskania remisji
Allogeniczny przeszczep komórek macierzystych może pełnić dwie funkcje
- Bardzo wysokie dawki chemioterapii eliminują chłoniaka, a nowe komórki dawcy umożliwiają regenerację układu odpornościowego, skracając czas, w którym układ odpornościowy nie działa. Nowe komórki dawcy przejmują rolę funkcji układu odpornościowego i produkcji zdrowych komórek krwi, takich jak limfocyty. Komórki macierzyste dawcy zastępują dysfunkcyjne komórki macierzyste pacjenta.
- Efekt przeszczepu kontra chłoniak. Wtedy komórki macierzyste dawcy (zwane przeszczepem) rozpoznają pozostałe komórki chłoniaka i atakują je, niszcząc chłoniaka. Jest to pozytywny efekt, gdy komórki macierzyste dawcy pomagają w leczeniu chłoniaka. Należy zauważyć, że ten efekt przeszczepu przeciwko chłoniakowi nie zawsze występuje w ten sposób. Chłoniak może być oporny na komórki macierzyste dawcy lub organizm biorcy (zwany gospodarzem) może walczyć z komórkami dawcy (zwanym przeszczepem), co skutkuje choroba przeszczep przeciwko gospodarzowi (powikłanie przeszczepu allogenicznego).
Proces allogenicznego przeszczepu komórek macierzystych składa się z pięciu etapów
Dr Amit Khot, hematolog i lekarz zajmujący się przeszczepami szpiku kostnego
Peter MacCallum Cancer Center i Royal Melbourne Hospital
- Przygotowanie: obejmuje to badania krwi w celu określenia rodzaju wymaganych komórek. Czasami ludzie potrzebują „ratunkowej” chemioterapii, aby spróbować zminimalizować chłoniaka przed przeszczepem.
- Pobieranie komórek macierzystych: jest to proces pobierania komórek macierzystych, ponieważ przeszczep allogeniczny pochodzi od dawcy, zespół medyczny musi znaleźć dopasowanie do przeszczepu.
- Kuracja kondycjonująca: jest to chemioterapia, terapia celowana i immunoterapia podawana w bardzo wysokich dawkach w celu wyeliminowania całego chłoniaka
- Reinfuzja komórek macierzystych: po podaniu leczenia wysokimi dawkami podaje się komórki macierzyste, które wcześniej pobrano od dawcy.
- Wszczepienie: jest to proces, w którym komórki macierzyste dawcy osiedlają się w organizmie i przejmują funkcjonowanie układu odpornościowego.
Przygotowanie do leczenia
Przygotowanie do przeszczepu komórek macierzystych będzie wymagało wielu przygotowań. Każdy przeszczep jest inny, a zespół transplantacyjny powinien zorganizować wszystko dla pacjenta. Niektóre przygotowania, których można się spodziewać, mogą obejmować:
Wprowadzenie linii centralnej
Jeśli pacjent nie ma jeszcze wkłucia centralnego, zostanie ono założone przed przeszczepem. Centralną linią może być PICC (cewnik centralny wprowadzony obwodowo). To może być CVL (centralna linia żylna). Lekarz zdecyduje, która linia centralna jest najlepsza dla pacjenta.
Linia centralna umożliwia jednoczesne przyjmowanie wielu różnych leków. Pacjenci na ogół potrzebują wielu różnych leków i badań krwi podczas przeszczepu, a linia centralna pomaga pielęgniarkom lepiej zarządzać opieką nad pacjentem.
Chemioterapia
Chemioterapia w dużych dawkach jest zawsze podawana jako część procesu transplantacji. Chemioterapia w wysokich dawkach nazywa się terapia kondycjonująca. Poza chemioterapią wysokodawkową niektórzy pacjenci potrzebują chemioterapii ratunkowej. Terapia ratunkowa ma miejsce, gdy chłoniak jest agresywny i musi zostać zredukowany, zanim reszta procesu przeszczepu będzie mogła się odbyć. Imię odzysk pochodzi z próby ratowania organizmu przed chłoniakiem.
Przeprowadzka na leczenie
Tylko niektóre szpitale w Australii są w stanie przeprowadzać allogeniczne przeszczepy komórek macierzystych. Z tego powodu może być konieczne przeniesienie się z domu w okolice bliższe szpitala. Większość szpitali transplantologicznych posiada pokoje dla pacjentów, w których może mieszkać pacjent i opiekun. Porozmawiaj z pracownikiem socjalnym w swoim ośrodku terapeutycznym, aby dowiedzieć się, jakie są możliwości zakwaterowania.
Zachowanie płodności
Przeszczep komórek macierzystych wpłynie na zdolność pacjentki do posiadania dzieci. Ważne jest, aby omówić dostępne opcje zachowania płodności.
Praktyczne wskazówki
Przeszczep komórek macierzystych zwykle wiąże się z długim pobytem w szpitalu. Pomocne może być spakowanie niektórych z tych rzeczy:
- Kilka par miękkich, wygodnych ubrań lub piżam i dużo bielizny.
- Szczoteczka do zębów (miękka), pasta do zębów, mydło, delikatny krem nawilżający, delikatny dezodorant
- Własna poduszka (umyj w gorącej wodzie poszewkę na poduszkę i wszelkie osobiste koce / dywaniki przed przyjęciem do szpitala – umyj je w gorącej wodzie, aby zredukować liczbę bakterii, ponieważ twój układ odpornościowy będzie bardzo wrażliwy).
- Kapcie lub wygodne buty i mnóstwo par skarpetek
- Przedmioty osobiste, które rozjaśnią salę szpitalną (zdjęcie bliskich)
- Artykuły rozrywkowe, takie jak książki, czasopisma, krzyżówki, iPad/laptop/tablet. Szpital może być bardzo nudny, jeśli nie masz nic do roboty.
- Kalendarz do śledzenia daty, długie pobyty w szpitalu mogą zamazać wszystkie dni razem.
HLA i typowanie tkankowe
W przypadku allogenicznego (dawczego) przeszczepu komórek macierzystych koordynator ds. transplantacji organizuje poszukiwanie odpowiedniego dawcy komórek macierzystych. Allogeniczny przeszczep komórek macierzystych ma największe szanse na powodzenie, jeśli komórki dawcy ściśle pasują do pacjenta. Aby to sprawdzić, pacjentowi zostanie wykonane badanie krwi tzw typowanie tkankowe który przygląda się różnym białkom na powierzchni komórek tzw antygeny ludzkich leukocytów (HLA).
Komórki każdego człowieka wytwarzają białka HLA, aby pomóc układowi odpornościowemu rozpoznawać komórki, które należą do organizmu i rozpoznawać komórki, które nie należą.
Istnieje wiele różnych typów HLA, a zespół medyczny stara się znaleźć dawcę, którego typy HLA są jak najbardziej zbliżone do własnych.
Jeśli to możliwe, starają się również upewnić, że pacjent i dawca byli narażeni na te same wirusy, chociaż jest to mniej ważne niż dopasowanie HLA.
Bracia lub siostry najprawdopodobniej mają białka HLA, które są podobne do pacjenta. Około 1 osoba na 3 ma brata lub siostrę, którzy dobrze do siebie pasują. Jeśli pacjent nie ma braci ani sióstr lub jeśli nie są one dobrze dopasowane, zespół medyczny będzie szukać dawcy ochotnika, którego typ HLA najbardziej pasuje do pacjentów. Jest to znane jako dopasowany niespokrewniony dawca (MUD), a miliony ochotników są zarejestrowane w krajowych i światowych rejestrach komórek macierzystych.
Jeśli nie zostanie znaleziony dopasowany niespokrewniony dawca (MUD) dla pacjenta, możliwe może być wykorzystanie innych źródeł komórek macierzystych. Obejmują one:
- Krewny, którego typ HLA w połowie pasuje do twojego: jest to znany jako „haploidentyczny” dawca
- Krew pępowinowa od niespokrewnionego dawcy: krew pępowinowa nie musi być tak ściśle dopasowana do twojego typu HLA, jak inne źródła komórek macierzystych. Jest bardziej prawdopodobne, że będzie stosowany u dzieci niż u dorosłych, ponieważ zawiera mniej komórek macierzystych niż inne źródła. Dostępne są rejestry przechowywanej krwi pępowinowej.
Kolekcja komórek macierzystych
Istnieją dwa sposoby, w jakie dawca może przekazać komórki macierzyste.
- Pobieranie komórek macierzystych krwi obwodowej
- Dawstwo komórek macierzystych szpiku kostnego
Dawstwo komórek macierzystych krwi obwodowej
Obwodowe komórki macierzyste są pobierane z krwi obwodowej. W ramach przygotowań do pobrania obwodowych komórek macierzystych większość osób otrzymuje zastrzyki z czynnikiem wzrostu. Czynniki wzrostu stymulują produkcję komórek macierzystych. Pomaga to komórkom macierzystym przemieszczać się ze szpiku kostnego do krwioobiegu, gdzie są gotowe do pobrania.
Pobieranie odbywa się poprzez oddzielenie komórek macierzystych od reszty krwi, a proces wykorzystuje maszynę do aferezy. Maszyna do aferezy może oddzielić różne składniki krwi i oddzielić komórki macierzyste. Po przejściu przez fazę zbierania komórek krew wraca do organizmu. Ten proces trwa kilka godzin (około 2 – 4 godzin). Dawca może wrócić do domu po zabiegu, jednak może być konieczne powrót następnego dnia, jeśli nie pobrano wystarczającej liczby komórek.
Afereza jest mniej inwazyjna niż pobieranie szpiku kostnego i częściowo dlatego jest preferowaną metodą pobierania komórek macierzystych.
W przeszczepach allogenicznych (dawczych) dawca poddawany jest aferezie dla biorcy, a pobranie to odbywa się jak najbliżej dnia przeszczepu. Ponieważ te komórki macierzyste zostaną dostarczone biorcy świeże w dniu przeszczepu.
Dawstwo komórek macierzystych szpiku kostnego
Mniej powszechnym podejściem do pobierania komórek macierzystych jest pobieranie szpiku kostnego. To tutaj komórki macierzyste są pobierane ze szpiku kostnego w znieczuleniu ogólnym. Lekarze wprowadzają igłę do kości w okolicy miednicy, zwanej grzebieniem biodrowym. Szpik kostny jest pobierany z miednicy przez igłę, a następnie jest filtrowany i przechowywany do dnia przeszczepu.
Krwi pępowinowej donacja pochodzi z publicznego banku pępowiny, w którym zostały przekazane i przechowywane komórki macierzyste z krwi pozostawionej w pępowinie i łożysku po urodzeniu dziecka.
Jak działa afereza
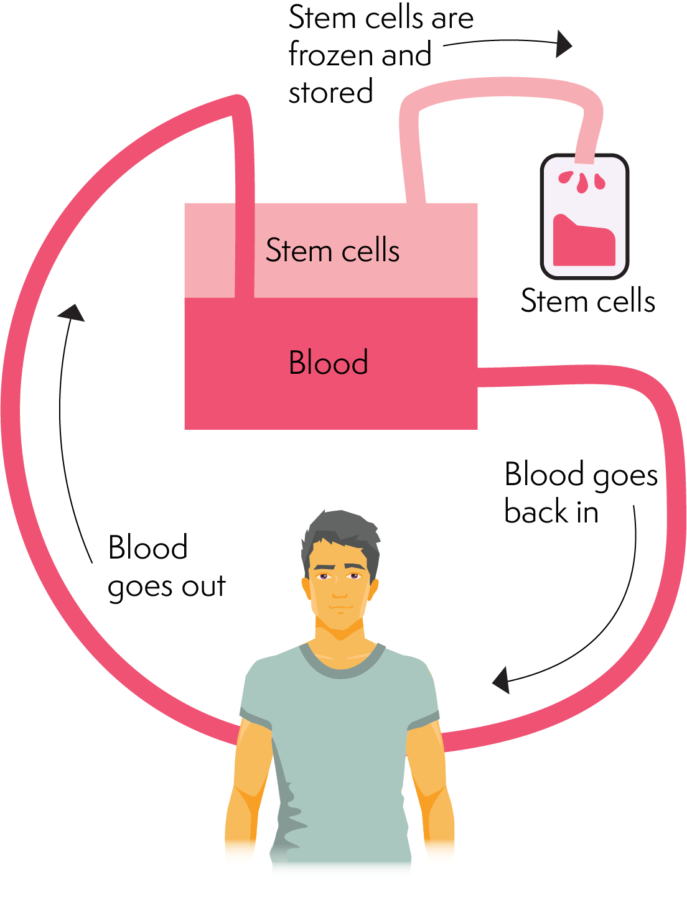
Przetwarzanie/konserwowanie komórek macierzystych lub szpiku kostnego
Komórki macierzyste pobrane do przeszczepu allogenicznego (dawcy) są pobierane bezpośrednio przed użyciem i nie są przechowywane przez dłuższy czas.
Komórki macierzyste pobrane do autologicznego (samodzielnego) przeszczepu są na ogół konserwowane i przechowywane w zamrażarce do czasu użycia.
Kondycjonowanie
Pacjenci poddawani przeszczepowi są najpierw poddawani leczeniu zwanemu schematem kondycjonowania. Jest to leczenie dużymi dawkami podawane na kilka dni przed wlewem komórek macierzystych. Terapia kondycjonująca może obejmować chemioterapię, a czasem radioterapię. Dwa cele terapii kondycjonującej to:
- Aby zabić jak najwięcej chłoniaków
- Zmniejsz populację komórek macierzystych
Istnieje wiele różnych kombinacji chemioterapii, radioterapii i immunoterapii, które można stosować w reżimach kondycjonowania. Istnieją różne intensywności zabiegów kondycjonujących, są to:
- Kondycjonowanie mieloablacyjne o pełnej intensywności
- Kondycjonowanie niemieloablacyjne
- Kondycjonowanie o zmniejszonej intensywności
We wszystkich schematach leczenie jest intensywne, w wyniku czego wraz z chłoniakiem obumiera wiele zdrowych komórek. Wybór schematu będzie zależał od rodzaju chłoniaka, historii leczenia i innych indywidualnych czynników, takich jak wiek, ogólny stan zdrowia i sprawność fizyczna. Zespół leczący omówi z pacjentem, który schemat kondycjonowania jest odpowiedni dla pacjenta.
W przypadku przeszczepu allogenicznego pacjenci mogą zostać przyjęci do szpitala już na 14 dni przed przeszczepem. Każdy przypadek pacjenta jest inny, a lekarz poinformuje Cię, kiedy zostaniesz przyjęty. Pacjenci pozostają w szpitalu od 3 do 6 tygodni po przeszczepie. To jest wskazówka; każdy przeszczep jest inny, a niektóre osoby wymagają dłuższej opieki medycznej dłużej niż 6 tygodni.
W przypadku allogenicznego przeszczepu komórek macierzystych z wykorzystaniem komórek macierzystych od dawcy niespokrewnionego lub dawcy o dużym stopniu niedopasowania, może być konieczne leczenie kondycjonujące o większej intensywności.
Możesz mieć inne leczenie kondycjonujące, jeśli masz allogeniczny przeszczep z wykorzystaniem komórek macierzystych z krwi pępowinowej lub od częściowo dopasowanego krewnego.
Możesz uzyskać dostęp do szczegółowych informacji na temat schematów kondycjonowania na stronie stronie internetowej firmy Eviq.
Reinfuzja komórek macierzystych
Po zakończeniu intensywnej chemioterapii kondycjonującej następuje reinfuzja komórek macierzystych. Te komórki macierzyste powoli zaczynają wytwarzać nowe, zdrowe komórki krwi. W końcu wyprodukują wystarczającą ilość zdrowych komórek, aby ponownie zaludnić cały szpik kostny, uzupełniając wszystkie komórki krwi i odpornościowe.
Ponowna infuzja komórek macierzystych jest prostą procedurą. Jest to podobne do transfuzji krwi. Komórki podaje się przez linię do linii centralnej. Dzień reinfuzji komórek macierzystych nazywany jest „Dniem Zero”.
Przy każdym zabiegu medycznym istnieje ryzyko wystąpienia reakcji na infuzję komórek macierzystych. U większości ludzi nie ma reakcji, ale u innych mogą wystąpić:
- Nudności lub bycie chorym
- Nieprzyjemny smak lub pieczenie w ustach
- Nadciśnienie
- Reakcja alergiczna
- Zakażenie
W allogenicznych przeszczepach komórek macierzystych, gdy te oddane komórki zatrzymują się (lub wszczepiają) w biorcę (pacjenta). Zaczynają funkcjonować jako część układu odpornościowego i mogą atakować komórki chłoniaka. To się nazywa efekt przeszczep przeciw chłoniakowi.
W niektórych przypadkach po przeszczepie allogenicznym komórki dawcy atakują również zdrowe komórki pacjenta. To się nazywa choroba przeszczep przeciwko gospodarzowi (GVHD).
Wszczepienie Twoich komórek macierzystych
Wszczepienie ma miejsce, gdy nowe komórki macierzyste zaczynają stopniowo przejmować rolę pierwotnych komórek macierzystych. Zwykle dzieje się to około 2-3 tygodni po infuzji komórek macierzystych, ale może to potrwać dłużej, zwłaszcza jeśli nowe komórki macierzyste pochodzą z krwi pępowinowej.
Podczas gdy nowe komórki macierzyste się wszczepiają, istnieje bardzo wysokie ryzyko infekcji. Ludzie na ogół muszą pozostać w szpitalu przez ten okres, ponieważ mogą zachorować i muszą mieć możliwość natychmiastowego poddania się leczeniu.
Czekając na poprawę liczby krwinek, możesz zastosować niektóre z poniższych metod leczenia, aby wspomóc powrót do zdrowia:
- Transfuzje krwi – w przypadku małej liczby czerwonych krwinek (niedokrwistości)
- Transfuzje płytek krwi – przy niskim poziomie płytek krwi (małopłytkowość)
- Antybiotyki – na infekcje bakteryjne
- Leki przeciwwirusowe – na infekcje wirusowe
- Leki przeciwgrzybicze – na infekcje grzybicze
Syndrom wszczepienia
Po otrzymaniu nowych komórek macierzystych u niektórych osób po 2-3 tygodniach pojawiają się następujące objawy, na ogół mniej więcej w czasie wszczepienia komórek:
- Gorączka: wysoka temperatura 38 stopni lub wyższa
- czerwona wysypka
- Biegunka
- Zatrzymanie płynów
Nazywa się to „syndromem wszczepienia”. Występuje częściej po samodzielnym (autologicznym) przeszczepie komórek macierzystych niż po przeszczepie komórek macierzystych od dawcy (alogenicznego).
Jest to częsty efekt uboczny przeszczepu i jest leczony sterydami. Objawy te mogą być również spowodowane innymi czynnikami, w tym chemioterapią, i mogą nie być oznaką zespołu wszczepienia.
Niektóre typowe protokoły szpitalne podczas przeszczepu obejmują:
- Zazwyczaj przebywasz w sali szpitalnej sam przez cały czas pobytu
- Sala szpitalna jest regularnie sprzątana, a pościel i poszewki na poduszki zmieniane są codziennie
- Nie możesz mieć żywych roślin ani kwiatów w swoim pokoju
- Personel szpitala i goście muszą umyć ręce przed wejściem do pokoju
- Czasami odwiedzający i personel szpitala mogą być zmuszeni do noszenia rękawiczek, fartuchów lub fartuchów oraz masek na twarz podczas wizyty u Ciebie
Ludzie nie powinni cię odwiedzać, jeśli są chorzy - Dzieci poniżej określonego wieku mogą w ogóle nie mieć pozwolenia na odwiedziny – chociaż niektóre szpitale zezwalają na nie, jeśli dzieci są zdrowe
Gdy liczba krwinek się poprawi, a stan pacjenta będzie wystarczająco dobry, będzie mógł wrócić do domu. Po tym czasie będą pod ścisłą obserwacją zespołu medycznego.
Powikłania po przeszczepie komórek macierzystych
Choroba przeszczep przeciwko gospodarzowi (GvHD)
Choroba przeszczep przeciwko gospodarzowi (GvHD) jest częstym powikłaniem allogenicznego przeszczepu komórek macierzystych. Dzieje się tak, gdy:
- Komórki T dawcy (nazywane również „przeszczepem”) rozpoznają antygeny na innych komórkach organizmu biorcy (zwanego „gospodarzem”) jako obce
- Po rozpoznaniu tych antygenów komórki T dawcy atakują następnie komórki swojego nowego gospodarza.
Efekt ten może być przydatny, gdy limfocyty T nowego dawcy atakują pozostałe komórki chłoniaka (nazywane efektem przeszczep przeciwko chłoniakowi). Niestety komórki T dawcy mogą również atakować zdrowe tkanki. Może to spowodować poważne skutki uboczne.
Przez większość czasu GvHD powoduje łagodne lub umiarkowane objawy, ale czasami może być ciężka, a nawet zagrażać życiu. Przed i po przeszczepie pacjenci otrzymują leczenie zmniejszające ryzyko rozwoju GvHD. Zespół transplantacyjny ściśle monitoruje pacjenta pod kątem jakichkolwiek objawów GvHD, aby móc leczyć go tak wcześnie, jak to możliwe, jeśli się rozwinie.
GvHD jest klasyfikowany jako „ostry” lub „przewlekły” w zależności od objawów przedmiotowych i podmiotowych.
Ryzyko infekcji
Po przeszczepie komórek macierzystych wysokie dawki chemioterapii wyeliminują wiele białych krwinek, w tym białe krwinki zwane neutrofilami. Niski poziom neutrofili jest znany jako neutropenia. Przedłużająca się neutropenia naraża osobę na bardzo wysokie ryzyko rozwoju infekcji. Infekcje można leczyć, jednak jeśli nie zostaną wcześnie wykryte i leczone natychmiast, mogą zagrażać życiu.
Podczas pobytu w szpitalu, bezpośrednio po przeszczepie komórek macierzystych, zespół leczący będzie podejmował środki ostrożności, aby zapobiegać rozwojowi infekcji, a także ściśle monitorował objawy infekcji. Chociaż podejmuje się wiele środków ostrożności w celu zmniejszenia ryzyka zarażenia się infekcją, większość pacjentów po allogenicznym przeszczepie komórek macierzystych zachoruje na infekcję.
W ciągu pierwszych kilku tygodni po przeszczepie pacjenci są najbardziej narażeni na rozwój infekcji bakteryjnej. Takie infekcje obejmują infekcje krwi, zapalenie płuc, infekcje układu pokarmowego lub infekcje skóry.
W ciągu najbliższych kilku miesięcy pacjenci są najbardziej narażeni na rozwój infekcji wirusowych i mogą to być wirusy, które były uśpione w organizmie przed przeszczepem i mogą wybuchnąć, gdy układ odpornościowy jest osłabiony. Nie zawsze powodują objawy. Po przeszczepie będą przeprowadzane regularne badania krwi, aby upewnić się, że zaostrzenie infekcji wirusowej zwanej wirusem cytomegalii (CMV) zostanie wcześnie wykryte. Jeśli badanie krwi wykaże obecność CMV – nawet jeśli nie ma objawów – pacjent zostanie poddany leczeniu lekami przeciwwirusowymi. Może być potrzebny więcej niż jeden cykl leczenia, a leczenie to może wydłużyć pobyt w szpitalu.
Liczba krwinek zaczyna rosnąć od 2 do 4 tygodni po allogenicznym przeszczepie komórek macierzystych. Jednak pełna regeneracja układu odpornościowego może zająć wiele miesięcy, a czasem nawet lat.
Podczas wypisu ze szpitala zespół medyczny powinien doradzić, na jakie objawy infekcji zwrócić uwagę iz kim się skontaktować, jeśli istnieje możliwość zakażenia lub cokolwiek innego, co może niepokoić pacjenta.
Skutki uboczne bardzo wysokich dawek chemioterapii
Pacjenci mogą doświadczyć skutków ubocznych leczenia przeciwnowotworowego dużymi dawkami. Następujące działania niepożądane mogą występować często, a więcej informacji znajduje się w skutki uboczne Sekcja
- Zapalenie błony śluzowej jamy ustnej (ból jamy ustnej)
- Niedokrwistość (mała liczba czerwonych krwinek)
- Małopłytkowość (mała liczba płytek krwi)
- Nudności i wymioty
- Problemy z przewodem pokarmowym (biegunka lub zaparcia)
Niepowodzenie przeszczepu
Niepowodzenie przeszczepu występuje, gdy przeszczepione komórki macierzyste nie osadzają się w szpiku kostnym i nie wytwarzają nowych krwinek. Oznacza to, że liczba krwinek nie wraca do normy lub zaczyna się poprawiać, ale potem ponownie spada.
Niepowodzenie przeszczepu jest poważne, ale zdarza się rzadko po allogenicznym przeszczepie komórek macierzystych, zwłaszcza jeśli dawca jest dobrze dopasowany.
Zespół medyczny będzie ściśle monitorował morfologię krwi, a jeśli nowa komórka macierzysta zacznie zawodzić, pacjent może być początkowo leczony hormonami czynnika wzrostu. Mogą one zachęcać komórki macierzyste w szpiku kostnym do wytwarzania większej liczby komórek.
Jeśli komórki macierzyste dawcy nie zostaną wszczepione, pacjent może potrzebować drugiego przeszczepu komórek macierzystych. Ten drugi przeszczep może pochodzić od tego samego dawcy komórek macierzystych lub od innego.
Późne efekty
Późne efekty to problemy zdrowotne, które mogą rozwinąć się miesiące lub lata po leczeniu chłoniaka. Większość ośrodków transplantologicznych ma dedykowane usługi w zakresie późnych skutków, które oferują programy badań przesiewowych w celu wykrycia późnych skutków tak wcześnie, jak to możliwe. Daje to pacjentowi największe szanse na pomyślne leczenie, jeśli wystąpią jakiekolwiek późne skutki.
Pacjenci mogą być również narażeni na ryzyko rozwoju zespołu limfoproliferacyjnego po przeszczepie (PTLD) – chłoniaków, które mogą rozwinąć się u osób przyjmujących leki immunosupresyjne po przeszczepie. Jednak PTLD występuje rzadko. U większości pacjentów po przeszczepach nie rozwija się PTLD.
Zachowaj ostrożność
Po przeszczepie komórek macierzystych będą odbywać się regularne (cotygodniowe) wizyty u lekarza. Kontynuacja będzie kontynuowana przez miesiące i lata po leczeniu, ale coraz rzadziej w miarę upływu czasu. W końcu lekarze transplantolodzy będą mogli przekazać dalszą opiekę lekarzowi pierwszego kontaktu.
Około 3 miesiące po przeszczepie, a Skanowanie zwierzęcia, tomografia komputerowa i / lub aspirat szpiku kostnego (BMA) można zaplanować, aby ocenić, jak przebiega ożywienie.
W tygodniach i miesiącach następujących po przeszczepie często trzeba wracać do szpitala na leczenie, ale wraz z upływem czasu zmniejsza się ryzyko poważnych powikłań.
Pacjenci mogą również doświadczać działań niepożądanych związanych z leczeniem dużymi dawkami i mogą czuć się źle i bardzo zmęczeni. Jednak zwykle powrót do zdrowia po przeszczepie komórek macierzystych trwa około roku.
Zespół medyczny powinien doradzić, jakie inne czynniki należy wziąć pod uwagę w okresie rekonwalescencji. Lymphoma Australia ma prywatną stronę internetową na Facebooku, Lymphoma Down Under, na której można zadawać pytania i uzyskać wsparcie od innych osób dotkniętych chłoniakiem lub przeszczepem komórek macierzystych.
Co dzieje się po przeszczepie komórek macierzystych?
Wykończenie leczenia może być trudnym okresem dla wielu pacjentów, ponieważ po przeszczepie wracają do życia. Niektóre z powszechnych obaw mogą dotyczyć:
- Fizyczny
- Psychiczne samopoczucie
- Zdrowie emocjonalne
- Relacje
- Praca, nauka i działalność społeczna
Informacja uzupełniająca
U Steve'a zdiagnozowano chłoniaka z komórek płaszcza w 2010 roku. Steve przeżył zarówno autologiczny, jak i allogeniczny przeszczep komórek macierzystych. To jest historia Steve'a.
Dr Nada Hamad, hematolog i lekarz zajmujący się przeszczepami szpiku kostnego
Szpital św. Wincentego w Sydney
Dr Amit Khot, hematolog i lekarz zajmujący się przeszczepami szpiku kostnego
Peter MacCallum Cancer Center i Royal Melbourne Hospital
Dr Amit Khot, hematolog i lekarz zajmujący się przeszczepami szpiku kostnego
Peter MacCallum Cancer Center i Royal Melbourne Hospital
Dr Amit Khot, hematolog i lekarz zajmujący się przeszczepami szpiku kostnego
Peter MacCallum Cancer Center i Royal Melbourne Hospital
Dr Amit Khot, hematolog i lekarz zajmujący się przeszczepami szpiku kostnego
Peter MacCallum Cancer Center i Royal Melbourne Hospital

